高中化学《铁盐和亚铁盐》
一、考题回顾

二、考题解析
【教学过程】
(一)生活导入
【提出问题】实验室当中的铁盐是什么颜色的?亚铁盐又是什么颜色的?
【学生回答】铁盐颜色是黄色的,亚铁盐是绿色的。
【教师引导】使得铁盐的颜色是黄色的,亚铁盐颜色是绿色的原因是什么?两者之间是否能够借助条件互相转换,这节课一同来探究以上几个问题。
(二)探究新知
【提出问题】回顾知识,铁盐显黄色的原因是什么?亚铁盐显蓝绿色的原因是什么?是否所有棕黄色的溶液都是铁盐溶液?
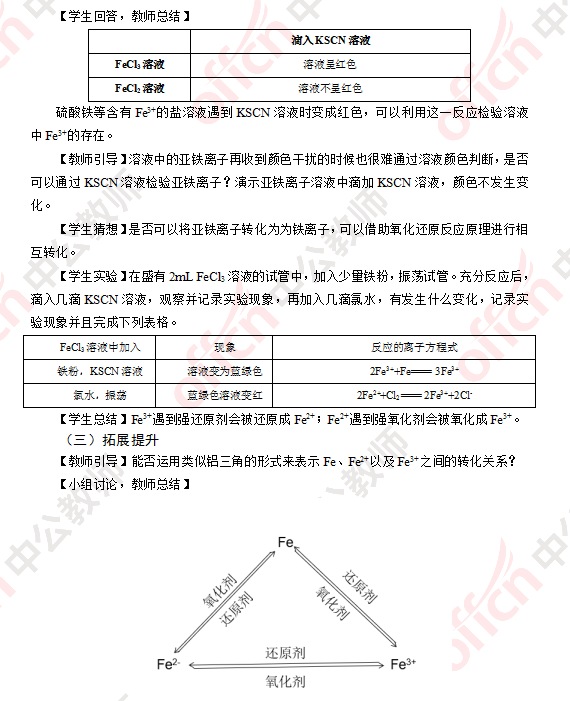
(四)小结作业
学生总结归纳本节课所学主要知识,表述学习心得。
作业:课下调研“铁三角”在生活生产中有哪些具体应用?
【板书设计】

【答辩题目解析】
1.鉴别铁离子和亚铁离子的方法都有哪些?
【参考答案】
直接观察颜色:含有亚铁离子的溶液呈浅绿色,含铁离子的溶液呈棕黄色。
利用显色反应:向溶液中滴加硫氰化钾溶液,溶液不显红色则是亚铁离子溶液,显红色的是铁离子溶液;向对比溶液中分别加苯酚,显紫色的溶液是铁离子溶液;向对比溶液中分别低价铁氰化钾,生成蓝色沉淀的是亚铁离子溶液,没有明显现象的是铁离子溶液。
利用氢氧化物沉淀的颜色:向对比溶液中分别滴加氢氧化钠溶液,生成白色沉淀之后迅速变成灰绿色最后变成红褐色的是亚铁离子溶液;直接生成红褐色沉淀的是铁离子溶液。
利用铁离子的氧化性:向对比溶液中分别加入铜片,无明显现象的为亚铁离子溶液;铜片被腐蚀,溶液变为蓝绿色的为铁离子溶液。同样原理使用淀粉碘化钾试纸以及硫化氢水溶液也能够鉴别出来。
2.本节课的教学重难点是什么?
【参考答案】
因为本节课具有实验探究性质,同时生活知识联系紧密,因此我制定本节课的教学重难点如下:
本节课的重点是学生能够学会鉴别三价铁离子的方式和方法,以及学会区分铁盐以及亚铁盐的方法。
本节课的教学难点是学生能够明确鉴别三价铁离子的操作过程,学会正规实验操作。
高中化学《电解质》
一、考题回顾

二、考题解析
【教学过程】
(一)生活导入
【提出问题】
①为什么出汗之后使用电器更容易发生触电事故?
②人体在剧烈运动之后为何要及时补充水分和盐分?
【学生回答】
①出汗后体表有更多的盐分,这些盐分在,汗起到了导电的作用;
②人体在剧烈运动之后,体内的Na、K和Cl伴随水分一起流失。
【教师引导】体内的Na、K和Cl伴随水分一起流失,出现电解质浓度失衡、紊乱,产生恶心、肌肉痉挛等症状,故需要及时补充电解质和水分。什么是电解质呢?这节课就来探究“电解质”。
(二)探究新知
【提出问题】根据我们的生活经验、已经学过的知识猜测哪些溶液导电,哪些不导电呢?设计相关学生实验
【学生实验】使用课前准备好的电源、导线、小灯泡及金属片进行HCl溶液、NaOH溶液、NaCl溶液、酒精溶液、蔗糖溶液的导电性实验。学生观察实验现象并记录实验结果。
【提出问题】实验结果中哪些溶液导电,哪些不导电呢?
【学生回答】导电的溶液:HCl溶液、NaOH溶液、NaCl溶液;不导电的溶液:酒精溶液、蔗糖溶液。
【播放视频】熔融的盐和酸导电的视频,学生观察现象。
【学生回答】灯泡变亮。
【教师总结】NaOH和NaCl不仅在水溶液中可以导电,加热至熔融状态也可以导电。在化学中将在水溶液或熔融状态下能够导电的化合物叫做电解质。并举例常见的酸、碱、盐中的电解质。
【学生回顾概念】电解质:在水溶液或熔融状态下能够导电的化合物。
【教师提问】PPT展示4个问题:
①金属、石墨可以导电,说明“C”是电解质,是否正确?
②盐酸可以导电,说明盐酸为电解质?
③硫酸钡不溶于水,因此硫酸钡不是电解质?
④二氧化碳、二氧化硫以及氨气溶于水导电,所以它们均为电解质?
【小组讨论,学生回答】总结出:
①“C”是单质,不是电解质;
②盐酸是氯化氢溶于水所得溶液,所以氯化氢为电解质,盐酸属于混合物,不在化合物的范畴;
③紧贴概念,硫酸钡在熔融状态下可导电,所以这一类难溶盐也属于电解质;
④二氧化碳、二氧化硫以及氨气与水反应所产生的物质溶于水导电,并非它们本身,所以二氧化碳、二氧化硫以及氨气不是电解质。(强调以上几点)
【教师提问】观看视频,并思考NaCl在水溶液或熔融状态下能够导电的原因?
【学生回答,教师总结】说明NaCl加入水中在水分子的作用下,钠离子和氯离子脱离NaCl晶体表面,进入水中,形成能够自由移动的水合钠离子及水合氯离子,这些离子在通电的作用下发生定向移动因此NaCl溶液可以导电。
NaCl晶体溶于水形成自由离子的的过程称为电离,通常用电离方程式表示,例:NaCl=Na++Cl-
(三)拓展提升

【答辩题目解析】
1.如何判断一个物质是电解质?
【参考答案】
电解质的定义是:在水溶液或熔融状态下能导电的化合物。那么判断是否为电解质可以根据以下三要素:①熔化或者溶解。②能导电。③化合物。
先判断是否属于化合物,电解质和非电解质都是化合物,其中电解质是指在熔融状态或在水溶液中由其本身电离出来的离子而导电的化合物,如果是化合物,接着再判断是否属于酸、碱、盐、水、活泼金属氧化物,如果是这几类物质的,则属于电解质;而非电解质则是在熔融状态和在水溶液中其本身均不能电离的化合物,例如:二氧化碳二氧化硫等所有非金属氧化物,蔗糖等有机物。
2.本节课的重难点是什么?在讲解中如何突出重点,突破难点?
【参考答案】
本节课的重难点都为:电离、电解质概念的形成和理解。所以在讲授中,1、对于电解质概念的形成,我首先采用了学生合作探究得出“电解质的概念”;随之就电解质相关的四个问题,让学生进行练习,从而加深学生对于电解质概念的理解;2、对于电离概念的形成,采用提问的方式,让学生带着问题观看视频,得出电离的概念,进而引出电离方程式,并让学生进行练习,进一步理解概念,从而达到突出重点、突破难点的目的。
高中化学《影响化学反应速率的因素》

二、考题解析
【教学过程】
(一)图片导入
【展示图片】面包的标签。请学生观察保质期。
【提出问题】根据生活常识知道在不同温度条件下,面包的保质期长短不同,那么温度是如何影响化学反应的快慢?除了温度还有哪些因素会影响化学反应的快慢呢?
(二)探究新知
【展示图片】请学生回忆初中学过的不同金属单质(镁、铝、锌、铁)与稀盐酸的反应。
【提出问题】在外界条件相同的情况下,不同的金属单质与稀盐酸反应,它们的快慢并不相同,这说明了什么?
【学生回答,教师总结】决定化学反应快慢的主要因素是反应物本身的性质。
【教师引导】那么外界条件对化学反应速率的影响是怎样的呢?能不能通过实验验证温度、催化剂、浓度对化学反应速率的影响呢?请同学们利用实验台上的药品、仪器等设计实验。接下来同学们以分好的实验小组为单位,讨论一下如何设计实验,7分钟之后请小组代表回答设计的方案。
(学生小组讨论环节)
【学生回答】①温度对化学反应速率的影响:控制其他外界条件相同,观察相同浓度的双氧水在不同温度下分解的反应速率;
②催化剂对化学反应速率的影响:控制其他外界条件相同,观察相同浓度的双氧水分别加入催化剂、不加入催化剂的反应速率;
③浓度对化学反应速率的影响:观察不同浓度的双氧水在相同条件的反应速率。
【教师引导】在做实验的时候注意控制好外界条件,各个小组按照自己小组设计的实验方案来进行实验,在实验的时候注意观察实验现象,并由此判断外界条件对化学反应速率的影响是怎样的。
(学生分组实验环节,教师巡视指导。)
【学生回答,小组总结】①温度对化学反应速率的影响:温度影响化学反应的速率,温度越高化学反应速率越快,反之越慢;
②催化剂对化学反应速率的影响:催化剂影响化学反应的速率,催化剂可以大大加快反应的速率;
③浓度对化学反应速率的影响:浓度影响化学反应的速率,浓度越大反应速率越大。
【提出问题】下列事实中,什么因素影响了化学反应的速率?
(1)铁矿石炼铁时要粉碎成矿粒。
(2)实验室进行化学反应时,常常把一些固体物质溶于水配成溶液再进行反应。
(3)工业合成氨,通常在2×107~5×107Pa的压强下进行。
【小组回答】
①反应物表面积:有固体参加的反应,固体的表面积越大,化学反应速率越快。
②反应物状态:通常气相或液相反应比固相反应的反应速率大。
③压强:对于有气体参加的反应,改变压强将使气体的体积发生改变,即相应地改变气体的浓度。
(三)拓展提升
【教师提问】在超市,为什么有很多的食品放置在冰柜当中,有什么作用?
【学生回答】通过降低温度有助于减慢化学反应速率,防止食品变质。
(四)小结作业
小结:总结影响化学反应速率的因素。
作业:调查生活生产中改变外界因素调节反应速率的实例,并用化学知识解释。

【答辩题目解析】
1.影响化学反应速率的因素有哪些?
【参考答案】
影响化学反应的速率分为内因和外因。内因是影响化学反应速率的本质也就是物质本身的性质,外因有反应物的浓度、温度、压强、催化剂。另外反应物的状态,比如块状还是粉末状,有没有搅拌等也会影响化学反应的速率。
2.教师如何评价学生?本堂课教学中你是如何对学生进行评价的?
【参考答案】
新课改理念要求教师注重对学生的情感、态度、价值观等方面进行综合评价。“评价”是学校教育教学活动中的一个重要环节。学校要建立评价学生全面发展的指标体系,不仅要关注学生的学业成绩,而且要注重发展和发现学生多方面的潜能和特长,如学生的道德品质、学习的愿望和能力、交流与合作、个性与情感以及创新意识和实践能力等。要采用灵活多样、具有开放性的评价方法,要关注过程性评价,帮助学生认识自我、建立自信,激发其内在的发展动力,使学生全面发展健康成长。本节课通过启发式的提问,引导学生思考,对于思考速度稍慢的同学我会耐心指导,在小组讨论中,我也会下去巡视,时时关注学生的讨论情况,并及时纠正和引导。
以上就是小编为您整理2018上半年高中化学教师资格证面试试题(精选)第三批的全部内容,更多精彩请进入教师资格栏目查看
只要一个电话
我们免费为您回电